
Rumus Kimia, Sifat Kebasaan (Alkalinitas), dan Bentuk Fisik Natrium Bikarbonat
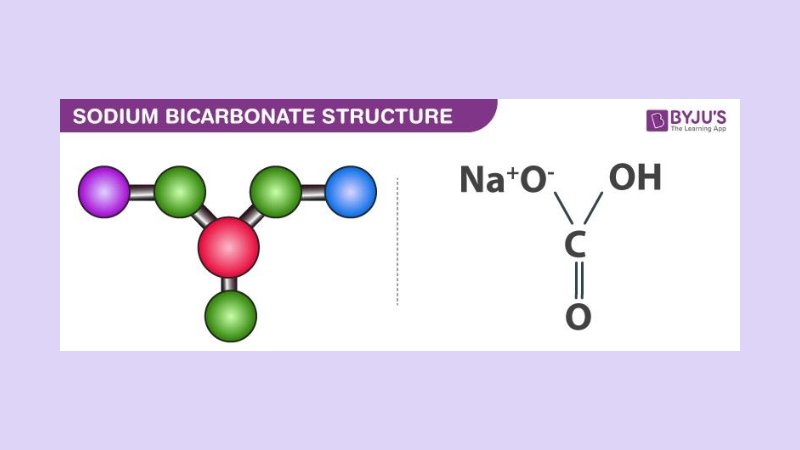
Natrium bikarbonat merupakan senyawa anorganik yang sangat dikenal dan banyak digunakan dalam berbagai bidang, mulai dari pangan, farmasi, hingga industri. Senyawa ini memiliki rumus kimia NaHCO₃, yang menunjukkan bahwa setiap satuan molekulnya tersusun atas satu kation natrium (Na⁺) dan satu anion bikarbonat (HCO₃⁻). Anion bikarbonat sendiri merupakan bentuk asam-basa amfoter dari sistem karbonat, yang berada di antara asam karbonat (H₂CO₃) dan ion karbonat (CO₃²⁻). Struktur ini menjadikan natrium bikarbonat memiliki sifat kimia yang relatif stabil namun tetap reaktif terhadap asam dan panas.
Dari sudut pandang sifat kebasaan (alkalinitas), natrium bikarbonat tergolong sebagai basa lemah. Ketika dilarutkan dalam air, senyawa ini tidak terdisosiasi sepenuhnya seperti basa kuat (misalnya natrium hidroksida), melainkan membentuk kesetimbangan. Ion bikarbonat akan bereaksi dengan molekul air menghasilkan ion hidroksida (OH⁻) dalam jumlah terbatas, sehingga larutan natrium bikarbonat memiliki pH yang bersifat sedikit basa, umumnya berada pada kisaran pH ±8,2–8,4 pada konsentrasi larutan jenuh. Alkalinitas ringan inilah yang membuat natrium bikarbonat cukup aman digunakan dalam aplikasi yang bersentuhan langsung dengan bahan pangan maupun tubuh manusia, karena tidak bersifat kaustik atau merusak jaringan.
Sifat kebasaan natrium bikarbonat juga bersifat buffering, artinya mampu menahan perubahan pH secara drastis ketika ditambahkan asam dalam jumlah tertentu. Ketika bereaksi dengan asam, ion bikarbonat akan menghasilkan karbon dioksida (CO₂), air (H₂O), dan garam natrium dari asam tersebut. Reaksi inilah yang mendasari berbagai pemanfaatannya, misalnya sebagai bahan pengembang, agen penetral asam, atau komponen dalam sistem pengatur pH. Namun, karena kebasaannya lemah, kapasitas penyangga pH natrium bikarbonat juga terbatas dan sangat bergantung pada konsentrasi serta kondisi lingkungan.
Secara fisik, natrium bikarbonat berbentuk serbuk kristalin putih dengan tekstur halus dan tidak berbau. Kristalnya tergolong kecil dan mudah menyerap kelembapan udara dalam tingkat tertentu, meskipun tidak se-higroskopis garam-garam alkali lainnya. Senyawa ini memiliki rasa sedikit asin dan agak basa jika bersentuhan dengan lidah. Kelarutannya dalam air bersifat sedang, yaitu sekitar 9–10 gram per 100 mL air pada suhu kamar, dan kelarutan tersebut meningkat dengan naiknya suhu. Dalam keadaan kering dan tersimpan baik, natrium bikarbonat relatif stabil, namun jika dipanaskan akan terurai menjadi natrium karbonat, air, dan karbon dioksida.
Reaksi Pengembang Kue
Mekanisme Reaksi Natrium Bikarbonat dengan Asam dan Panas dalam Menghasilkan Gas Karbon Dioksida (CO₂)
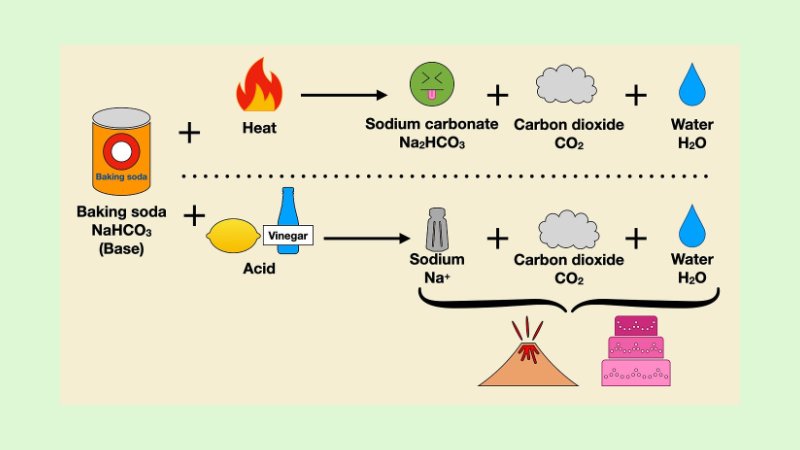
Natrium bikarbonat (NaHCO₃) berperan sebagai agen pengembang kimia melalui kemampuannya menghasilkan gas karbon dioksida (CO₂) ketika mengalami reaksi kimia tertentu. Proses pembentukan gas inilah yang menjadi dasar pengembangan adonan pada produk pangan seperti roti cepat saji, kue, dan biskuit. Secara kimia, terdapat dua mekanisme utama yang memungkinkan natrium bikarbonat melepaskan CO₂, yaitu reaksi dengan bahan asam dan dekomposisi akibat pemanasan. Kedua mekanisme ini dapat berlangsung secara terpisah maupun bersamaan, tergantung pada komposisi dan kondisi adonan.
Pada mekanisme pertama, natrium bikarbonat bereaksi dengan senyawa asam yang terdapat dalam adonan, misalnya asam asetat, asam sitrat, asam laktat, atau garam asam seperti krim tartar. Dalam lingkungan berair, natrium bikarbonat terdisosiasi menjadi ion natrium (Na⁺) dan ion bikarbonat (HCO₃⁻). Ion bikarbonat kemudian bereaksi dengan ion hidrogen (H⁺) yang dilepaskan oleh asam. Reaksi ini menghasilkan asam karbonat (H₂CO₃) yang bersifat tidak stabil dan segera terurai menjadi air (H₂O) dan gas karbon dioksida (CO₂). Gas CO₂ yang terbentuk akan muncul sebagai gelembung-gelembung kecil di dalam matriks adonan.
Gelembung CO₂ tersebut terperangkap oleh struktur adonan yang bersifat viskoelastis, terutama oleh jaringan protein (seperti gluten pada adonan berbasis tepung terigu) atau oleh matriks pati dan lemak. Ketika jumlah gas meningkat, tekanan internal di dalam adonan juga meningkat, sehingga adonan mengalami pengembangan volume. Semakin merata dan terkendali pembentukan CO₂, semakin baik tekstur akhir produk yang dihasilkan. Oleh karena itu, keberadaan bahan asam dalam jumlah yang seimbang sangat penting untuk memastikan seluruh natrium bikarbonat bereaksi secara optimal tanpa meninggalkan residu bersifat basa.
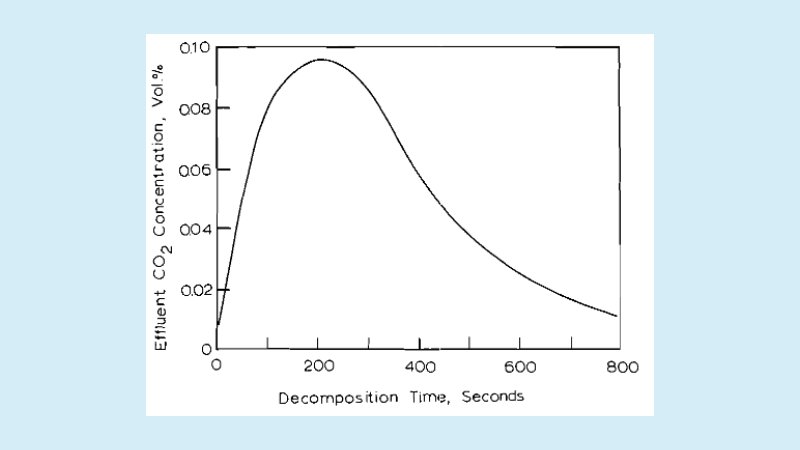
Mekanisme kedua melibatkan pengaruh panas. Ketika natrium bikarbonat dipanaskan hingga suhu tertentu (umumnya di atas ±80–100 °C), senyawa ini akan mengalami dekomposisi termal. Dalam proses ini, dua molekul natrium bikarbonat terurai membentuk satu molekul natrium karbonat (Na₂CO₃), satu molekul air, dan satu molekul gas karbon dioksida. Gas CO₂ yang dilepaskan kembali berperan sebagai agen pengembang, sedangkan natrium karbonat yang tersisa bersifat lebih basa dibandingkan natrium bikarbonat semula.
Dalam praktik pengolahan pangan, kedua mekanisme ini sering terjadi secara bersamaan. Reaksi dengan asam dapat dimulai sejak adonan dibasahi, sedangkan dekomposisi termal berlangsung lebih intens saat proses pemanggangan. Kombinasi ini memungkinkan pelepasan CO₂ terjadi secara bertahap, sehingga adonan dapat mengembang secara stabil sebelum struktur akhirnya mengeras akibat pemanasan lebih lanjut.
Peta Kegunaan Rumah Tangga

Pemetaan Kegunaan Praktis Natrium Bikarbonat di Rumah Tangga
Natrium bikarbonat (NaHCO₃) merupakan salah satu bahan kimia rumah tangga yang paling serbaguna karena sifat fisik dan kimianya yang relatif aman, bersifat basa lemah, serta mampu bereaksi dengan asam dan panas. Dalam konteks penggunaan domestik, natrium bikarbonat dimanfaatkan bukan hanya sebagai bahan pangan, tetapi juga sebagai agen pembersih, penyerap bau, hingga alat pemadam api ringan dalam kondisi tertentu. Kegunaan-kegunaan ini muncul dari kombinasi sifat abrasif ringan, kemampuan menetralkan asam, serta pelepasan gas karbon dioksida (CO₂).
Sebagai pembersih noda, natrium bikarbonat bekerja melalui dua mekanisme utama. Pertama, struktur kristalnya yang halus memberikan efek abrasif ringan yang mampu mengangkat kotoran tanpa merusak permukaan. Kedua, sifat alkalinitasnya membantu melonggarkan noda yang bersifat asam atau berminyak, sehingga lebih mudah terlepas saat digosok dengan air. Karena tidak bersifat korosif, natrium bikarbonat sering digunakan pada permukaan dapur, peralatan makan, hingga kain.
Dalam fungsi penghilang bau, natrium bikarbonat bekerja melalui mekanisme penetralan kimia. Bau tidak sedap umumnya disebabkan oleh senyawa volatil yang bersifat asam atau basa kuat. Natrium bikarbonat mampu bereaksi dengan senyawa asam tersebut, menurunkan volatilitasnya, dan dengan demikian mengurangi persepsi bau. Oleh karena itu, senyawa ini banyak ditempatkan di lemari es, tempat sampah, sepatu, atau karpet untuk menyerap bau tanpa menambahkan aroma lain.
Selain itu, natrium bikarbonat juga dikenal sebagai pemadam api ringan untuk kebakaran skala kecil, khususnya kebakaran akibat minyak atau lemak. Ketika dipanaskan secara cepat, natrium bikarbonat terurai dan melepaskan gas CO₂ yang bersifat inert terhadap proses pembakaran. Gas ini membantu mengurangi kadar oksigen di sekitar sumber api, sehingga nyala api dapat padam. Meskipun tidak menggantikan alat pemadam profesional, sifat ini menjelaskan mengapa natrium bikarbonat pernah digunakan dalam formulasi awal alat pemadam api kering.
Berikut tabel yang memetakan berbagai kegunaan praktis natrium bikarbonat di rumah beserta prinsip kimia yang mendasarinya:
| Kegunaan Rumah Tangga | Contoh Aplikasi | Prinsip Kimia Utama | Hasil yang Diperoleh |
|---|---|---|---|
| Pembersih noda | Membersihkan wastafel, kompor, peralatan dapur | Abrasif ringan dan basa lemah | Noda terangkat tanpa merusak permukaan |
| Penghilang bau | Lemari es, sepatu, karpet | Netralisasi senyawa asam volatil | Bau berkurang atau hilang |
| Pembersih kain | Mengurangi noda dan bau pada pakaian | Penyetaraan pH dan pelonggaran ikatan noda | Kain lebih bersih dan segar |
| Pembersih saluran air ringan | Mengurangi endapan dan bau | Reaksi dengan asam menghasilkan CO₂ | Endapan melonggar dan bau berkurang |
| Pemadam api ringan | Api kecil akibat minyak atau lemak | Dekomposisi termal menghasilkan CO₂ | Api meredup akibat penurunan oksigen |
| Agen penggosok lembut | Membersihkan keramik dan logam | Kristal halus tidak korosif | Permukaan bersih dan tidak tergores |
Kombinasi sifat kimia dan fisik tersebut menjadikan natrium bikarbonat sebagai contoh klasik senyawa sederhana dengan spektrum kegunaan rumah tangga yang luas, efektif, dan mudah diaplikasikan dalam kehidupan sehari-hari.
Manfaat Kesehatan (Antasida)
Cara Kerja Natrium Bikarbonat dalam Menetralkan Asam Lambung Berlebih dan Meredakan Heartburn
Natrium bikarbonat (NaHCO₃) dikenal luas sebagai antasida sederhana yang bekerja dengan mekanisme kimia langsung untuk menetralkan kelebihan asam lambung. Asam lambung terutama tersusun atas asam klorida (HCl), yang secara fisiologis berfungsi membantu pencernaan protein dan membunuh mikroorganisme. Namun, ketika produksi atau paparan asam ini berlebihan—misalnya akibat refluks asam ke kerongkongan—dapat timbul gejala seperti nyeri dada terbakar, rasa panas di tenggorokan, dan ketidaknyamanan yang dikenal sebagai heartburn.
Secara kimia, natrium bikarbonat adalah basa lemah yang sangat reaktif terhadap asam kuat seperti HCl. Ketika natrium bikarbonat masuk ke dalam lambung, senyawa ini segera larut dalam cairan lambung dan terdisosiasi menjadi ion natrium (Na⁺) dan ion bikarbonat (HCO₃⁻). Ion bikarbonat inilah yang berperan langsung dalam proses penetralan. Ion HCO₃⁻ akan bereaksi dengan ion hidrogen (H⁺) yang berasal dari asam klorida, membentuk asam karbonat (H₂CO₃), suatu senyawa antara yang tidak stabil.
Asam karbonat yang terbentuk kemudian dengan cepat terurai menjadi air (H₂O) dan gas karbon dioksida (CO₂). Reaksi ini menurunkan konsentrasi ion H⁺ bebas di dalam lambung, sehingga pH lambung yang semula sangat asam menjadi sedikit lebih netral. Penurunan keasaman inilah yang secara langsung mengurangi iritasi pada mukosa lambung dan kerongkongan, sehingga sensasi terbakar dan nyeri yang menyertai heartburn dapat mereda dalam waktu relatif singkat.
Efek kerja natrium bikarbonat bersifat cepat tetapi sementara. Hal ini disebabkan oleh dua faktor utama. Pertama, reaksi netralisasi berlangsung segera setelah kontak dengan asam lambung, sehingga memberikan kelegaan cepat. Kedua, hasil reaksi berupa CO₂ dapat meningkatkan tekanan gas di lambung, yang pada sebagian kasus dapat memicu sendawa. Gas ini kemudian dikeluarkan dari saluran pencernaan, sementara lambung tetap mampu memproduksi asam kembali sesuai mekanisme fisiologis normal.
Dari sudut pandang kimia-fisiologis, natrium bikarbonat tidak menghambat produksi asam lambung, melainkan hanya menetralkan asam yang sudah ada. Oleh karena itu, senyawa ini berbeda dari obat yang bekerja dengan mengurangi sekresi asam. Mekanisme kerja yang sederhana ini menjelaskan mengapa natrium bikarbonat telah lama digunakan sebagai antasida tradisional: reaksinya dapat diprediksi, produknya relatif tidak berbahaya, dan efek penurunan keasaman dapat dirasakan dengan cepat pada kondisi kelebihan asam lambung yang memicu heartburn.
Penggunaan dalam Olahraga

Konsep Soda Loading pada Atlet untuk Menunda Kelelahan Otot akibat Penumpukan Asam Laktat
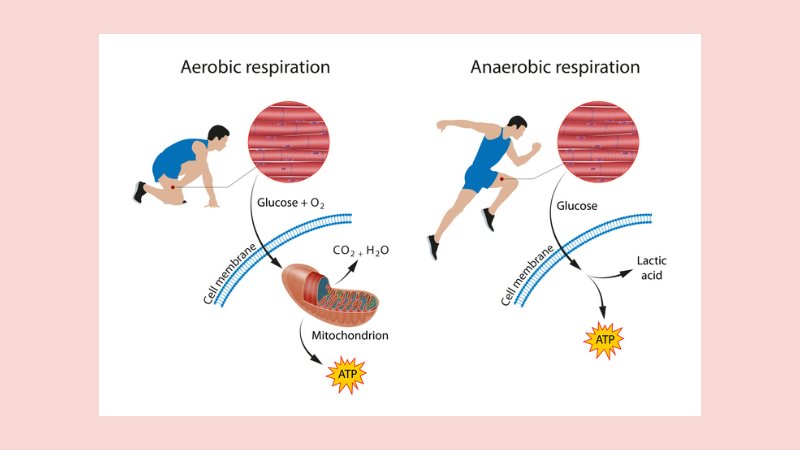
Konsep soda loading merujuk pada pemanfaatan natrium bikarbonat (NaHCO₃) sebagai agen penyangga (buffer) untuk menunda kelelahan otot yang muncul selama aktivitas fisik intensitas tinggi. Kelelahan ini secara fisiologis berkaitan erat dengan penurunan pH otot dan darah akibat akumulasi ion hidrogen (H⁺) yang dihasilkan selama metabolisme anaerob, terutama pada aktivitas yang menuntut kerja cepat dan eksplosif seperti lari jarak pendek, bersepeda sprint, atau latihan interval intensitas tinggi.
Dalam kondisi normal, otot menghasilkan energi melalui jalur aerob dan anaerob. Ketika kebutuhan energi meningkat secara drastis dan suplai oksigen tidak mencukupi, sel otot akan lebih banyak mengandalkan glikolisis anaerob. Proses ini menghasilkan asam laktat, yang kemudian terdisosiasi menjadi laktat dan ion H⁺. Penumpukan ion H⁺ inilah yang menyebabkan asidosis metabolik lokal, ditandai dengan penurunan pH intraseluler. Lingkungan yang semakin asam akan mengganggu kerja enzim, menghambat interaksi aktin–miosin, serta menurunkan kemampuan serabut otot berkontraksi secara optimal, sehingga muncul sensasi nyeri dan kelelahan.
Natrium bikarbonat berperan dalam konteks ini melalui sistem penyangga bikarbonat dalam darah. Ketika kadar bikarbonat dalam plasma meningkat, kapasitas darah untuk menetralkan ion H⁺ juga meningkat. Secara kimia, ion bikarbonat (HCO₃⁻) akan bereaksi dengan ion H⁺ membentuk asam karbonat (H₂CO₃), yang kemudian terurai menjadi air dan karbon dioksida. Karbon dioksida selanjutnya dikeluarkan melalui sistem pernapasan. Mekanisme ini membantu menjaga pH darah tetap lebih stabil meskipun produksi ion H⁺ meningkat selama latihan intens.
Dalam konsep soda loading, peningkatan kadar bikarbonat dalam darah menciptakan gradien pH antara otot dan darah. Gradien ini mendorong difusi ion H⁺ dari dalam sel otot ke aliran darah dengan lebih efisien. Akibatnya, lingkungan intraseluler otot menjadi relatif kurang asam dibandingkan kondisi tanpa penyangga tambahan. Dengan berkurangnya tingkat keasaman di dalam sel otot, proses kontraksi dapat dipertahankan lebih lama, dan kelelahan yang disebabkan oleh asidosis dapat tertunda.
Efek fisiologis ini menjelaskan mengapa soda loading sering dikaitkan dengan peningkatan performa pada aktivitas yang berdurasi singkat hingga menengah namun berintensitas tinggi. Perannya bukan sebagai sumber energi, melainkan sebagai modulator lingkungan kimia tempat reaksi metabolik dan mekanik otot berlangsung. Dengan menunda penurunan pH kritis, natrium bikarbonat secara tidak langsung memungkinkan atlet mempertahankan output tenaga yang tinggi sebelum kelelahan otot mencapai titik pembatas fungsional.



